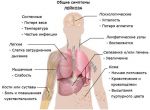
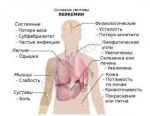
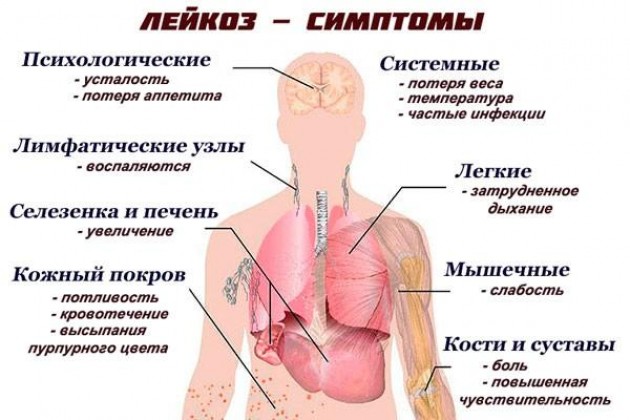
Лейко́з (греч. λευκός — белый) (лейкеми́я (греч. λευκός — белый и греч. αἷμα — кровь), алейкеми́я[3], белокровие, рак крови) — клональное злокачественное (неопластическое) заболевание кроветворной системы. К лейкозам относится обширная группа заболеваний, различных по своей этиологии. При лейкозах злокачественный клон может происходить как из незрелых гемопоэтических клеток костного мозга, так и из созревающих и зрелых клеток крови.
Причины лейкоза
В мире до сих пор ведутся исследования, результаты которых могли бы пролить свет на механизмы развития рака крови. В настоящее время специалисты заявляют о нескольких факторах, которые могут спровоцировать развитие заболевания. Это:
- радиация, избыточная инсоляция;
- воздействие химических соединений, которые оказывают мутагенный эффект;
- хромосомные дефекты;
- нарушения обменных процессов.
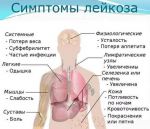
- 16 тихих признаков лейкемии, которые …
- Фибром лейкемия. Как называется рак …
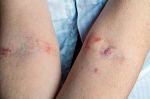
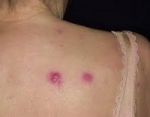
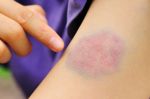
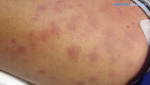
- Кожные проявления лейкозов
- 16 тихих признаков лейкемии, которые …
- Хронический лейкоз крови: лечение …
В группе риска находятся люди, которые проживают в зоне радиоактивного загрязнения или проходят лучевую терапию. Злокачественную трансформацию кровяных клеток может вызвать бензол, препараты с цитостатическим эффектом. Повышенная вероятность лейкемии наблюдается у пациентов с болезнью Дауна, синдромом Луи-Бар. Некоторые виды гемобластозов обусловлены воздействием ретровирусов и неправильным усвоением триптофана.
Диагностика Острого миелоидного лейкоза (острого нелимфобластного лейкоза, острого миелогенного лейкоза):
Диагноз ОМЛ устанавливается в более 30% случаев определения бластов в костном мозгу. Бласты должны иметь морфологическую и цитохимическую характеристику одного из FAB вариантов ОМЛ.
Цитохимические данные, направленные на диагностику вариантов заболевания, — положительная реакция на миелопероксидазу, с суданом черным Б и неспецифическую эстеразу, ингибируемую фтористым натрием. При этом совокупность данных показателей различается при разных вариантах ОМЛ. Так, наличие положительной реакции на миелопероксидазу характерно для вариантов М1, М2, М3 и М4, а неспецифическая эстераза, ингибируемая фтористым натрием, специфична для вариантов М4 и М5.
Существенным дополнением для диагностики ОМЛ являются иммунофенотипические исследования, уточняющие стандартную морфологическую диагностику и варианты ОМЛ.
Наиболее распространенными и широко применяемыми для подтверждения нелимфоидной природы лейкоза являются антигены CD13 и CD33, несколько реже используется CD65. Оценка этих трех маркеров позволяет подтвердить миелоидную природу опухолевых клеток в 98% случаев ОМЛ у детей.
Хромосомный анализ необходим для прогнозирования результатов лечения ОМЛ. Приблизительно у 75% детей, больных ОМЛ, можно выявить ту или иную хромосомную аберрацию, среди которых есть аномалии, характерные лишь для определенных вариантов ОМЛ. Так, t(8;21) ассоциируется с М2-вариантом, t(15;17) — с М3-вариантом, inv(16) — с М4-вариантом с эозинофилией. Аномалия 11q23 встречается при вариантах М4 и М5 и t(1;22) при М7-варианте. С помощью методов молекулярно-биологической диагностики — полимеразной цепной реакции (ПЦР) и FISH (fluorescent in situ hybridization) — можно определить хромосомную аберрацию, не выявленную при стандартном цитогенетическом исследовании. Это особенно важно для выбора определенного вида лечения в случае подтверждения М3-варианта. Кроме того, благодаря внедрению методов молекулярной диагностики ОМЛ в настоящее время у больных можно констатировать не только клинико-гематологическую, но и молекулярную ремиссию с последующим слежением за минимальной остаточной болезнью и определением молекулярного рецидива.
Основы классификации
Изначально лейкоз делили на «острый» и «хронический», имея в виду не характер течения заболевания, как это принято в других направлениях медицины, а предполагаемую продолжительность жизни пациента. В последних классификациях лейкозы различают по двум основным критериям:
- Клеточный фенотип — совокупность всех происходящих в клетке процессов.
- Степень дифференциации на момент клинических проявлений. Все разнообразные клетки организма берут общее начало от стволовых. По мере своего созревания они постепенно приобретают узкую специализацию. Чем выше степень дифференциации, тем клетка больше отличается от стволовых предшественников
Таким образом, выделяют 4 основных лейкоза, каждый из которых делится на множество подтипов:
- Острый лимфоцитарный лейкоз — самое распространенное онкологическое заболевание у детей. Представлен незрелыми и аномально долго живущими лимфоцитами.
- Хронический лимфоцитарный лейкоз. Чаще встречается в зрелом и пожилом возрасте. Представлен атипичными, но морфологически созревшими лимфоцитами.
- Острый миелоцитарный лейкоз — самый распространенный лейкоз у взрослых, который может носить вторичный характер. Представлен клетками-предшественниками миелоидного ряда — гранулоцитов и моноцитов.
- Хронический миелоцитарный лейкоз. Встречается в любом возрасте и представлен большим количеством незрелых клеток миелоидного ряда.
В отдельную группу выделяют так называемые миелодиспластические синдромы — целую группу заболеваний, при которых наблюдается неправильное развитие (дисплазия) клеток-предшественников различных линий кроветворения и дефицит зрелых форменных элементов в крови. У пациентов с такими заболеваниями повышается риск развития острого миелоидного лейкоза, но у большинства больных этого не случится.
Различные типы лейкоза имеют свои особенности, обусловливающие клиническую картину, течение заболевания, прогноз для жизни. Возможны бластные кризы, при которых заболевание приобретает характеристики острой патологии и угрожает жизни пациента.
Литература
- Медиафайлы на Викискладе
- Герценштейн Г. М. Белокровие // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Патологическая анатомия. Курс лекций / Под ред. В. В. Серова, М. А. Пальцева. — М.: Медицина, 1998. — 640 с. — 15 000 экз. — ISBN 5-225-02779-2, УДК 616, ББК
- Масчан М. А. и др. Что важно знать о лейкозах и об их лечении. Москва, 2011.
- Фигель М. Эпидемиология, патогенез и этиология острого лейкоза. Пер. с англ. Н. Д. Фирсовой (2017).
- Лейкоз: типы, симптомы и методы лечения …
- Лечение лейкоза в Германии цены …
- Лечение острого лейкоза и прогнозы …
- Рак крови (лейкоз): лечение народными …
- Лейкемия – что это за болезнь …