Раковая опухоль подразумевает появление в организме человека злокачественного новообразования, которое забирает часть питательных веществ себе и ухудшает общее состояние больного. Не секрет, что раковые опухоли — это бич современного общества. Однако благодаря науке, человечество значительно продвинулось в изучении этого недуга, и на сегодняшний день имеется немало информации о злокачественных образованиях.
Почему рак так называется
То что пациенты называют раком, на языке медицины означает онкологическое заболевание или злокачественную опухоль. Опухоль, неоплазия или новообразование — это скопление атипичных, неправильных клеток, которые бесконтрольно делятся и отказываются умирать.
Древнегреческий врач и философ Гиппократ одним из первых описал злокачественные новообразования. В своих трудах он дал им название karkinos, что в переводе с греческого означает «рак»: в разрезе крупные опухоли напоминали ему раков.
Позже древнеримский врач Корнелий Цельс перевел термин на латинский язык — так появилось современное название cancer. Другой римский медик и хирург Клавдий Гален описывал доброкачественные опухоли словом oncos. Сегодня онкология — наука, которая изучает механизм образования доброкачественных и злокачественных опухолей, методы их профилактики и принципы лечения.
В медицинской среде «рак» — это только карцинома, злокачественная опухоль из эпителиальной ткани.
Помимо карциномы к злокачественным опухолям относится саркома, меланома, лейкоз и лимфома. Саркома — злокачественная опухоль из соединительной ткани. К соединительной ткани относятся мышцы, связки, хрящи, суставы, кости, сухожилия, глубокие слои кожи. Меланома — злокачественная опухоль из меланоцитов (клеток кожи). Лейкоз или лейкемия — злокачественное новообразование кроветворной ткани, а лимфома — лимфатической.
Разновидности и свойства опухолей
Почему же точную причину так сложно установить? Ответ прост — существует множество разновидностей злокачественных опухолей, каждая из которых уникальна. Для облегчения классификации, новообразования принято подразделять в зависимости от типа поражённых клеток.
На данный момент выделяют следующие виды опухолей:
- Карцинома — клетки эпителия.
- Саркома — соединительная ткань, кости и мышцы.
- Меланома — если опухоль состоит из меланоцитов (клеток, ответственных за цвет кожи).
- Лимфома — лимфатическая ткань.
- Глиома — растёт из глиальных клеток головного мозга.
- Тератома — т. н. «зародышевые» клетки.
- Лейкоз — стволовые клетки головного мозга.
- Злокачественная опухоль — Википедия
- Рак шеи: симптомы, признаки …
- Лечение рака печени в Германии
- Опухоли. Опухолевый процесс — online …
- Обзор 4 перспективных методов для …
- Доброкачественные опухоли легких и …
Несмотря на огромные различия, все раковые новообразования имеют те или иные характерные признаки:
- Нетипичное строение клеток.
- Быстрый и неконтролируемый рост, приводящий к разрушению или сдавливанию здоровых органов и тканей.
- Возможность распространения на окружающие ткани.
- Склонность к образованию метастаз (местных патологических очагов опухоли) на соседних или отдалённых органах.
- Выработка токсинов, ослабляющих иммунитет, а также приводящих к физическому истощению и исхуданию.
- Маскировка под здоровую ткань (для обмана защитных сил организма).
- Высокая вероятность мутации.
- Наличие в основном молодых клеток.
- Ускоренное наполнение кровеносными сосудами.
II. Инвазивный дольковый рак молочной железы
Инвазивный дольковый рак составляет до 15% всех форм инвазивного РМЖ. По нашим наблюдениям его истинная частота выше, особенно с учетом наличия полей долькового рака в опухолях с преобладающим протоковым строением. Последние 20 лет ряд исследователей отмечают повышение частоты долькового РМЖ у женщин в возрасте младше 50 лет, особенно у применяющих гормонзаместительную терапию [1, 206, 207].
Нет существенных особенностей клинического течения этого варианта рака, хотя отмечено более частое вовлечение центральных отделов молочной железы, а также мультицентричное или билатеральное поражение [208].
Иногда возникают трудности диагностики этой опухоли. Это обусловлено спецификой гистологического строения долькового рака в отдельных случаях. Прежде всего это наличие массивных полей фиброза в скиррозных подвариантах опухоли, что не позволяет получить информативный материал при пункционной биопсии. Частый мультицентричный тип роста опухоли, состоящей из очень мелких очагов поражения, затрудняет проведение прицельной биопсии.
Пролиферативная активность долькового РМЖ обычно более низкая, чем протокового. Гиперэкспрессию онкобелка HER-2/neu отмечают крайне редко и только в плеоморфном подварианте долькового рака [1, 209, 210].
Исследование долькового рака с помощью проточной цитометрии позволило получить данные, свидетельствующие о том, что около 50% случаев долькового РМЖ являются диплоидными. Другие методы исследования, такие как цитогенетические или сравнительная геномная гибридизация, подтвердили снижение частоты хромосомных аномалий в дольковом раке по сравнению с протоковым. Наиболее частым геномным изменением долькового рака является потеря длинного плеча 16-й хромосомы (выявляют в 63–87% всех случаев).
Ген, кодирующий Е-кадгерин, находится в локусе 16q22. Нормальная работа этого гена обусловливает образование белка, обеспечивающего адгезию зрелого эпителия и дифференцировку клеток. Выявлена четкая корреляция между делецией 16q и потерей экспрессии Е-кадгерина. Данные иммуногистохимического исследования долькового рака свидетельствуют о том, что в 80–100% случаев происходит полная потеря способности к синтезу указанного белка. В то же время при протоковом раке данные изменения отмечают только в 30–60% случаев. Учитывая результаты молекулярного анализа, можно отметить, что отсутствие экспрессии к Е-кадгерину в раковых клетках коррелирует с мутацией в сочетании с инактивацией аллеля дикого типа [1, 211]. Альтернативные механизмы также могут вызывать повреждение самого белка и/или кадгеринассоциированных белков.
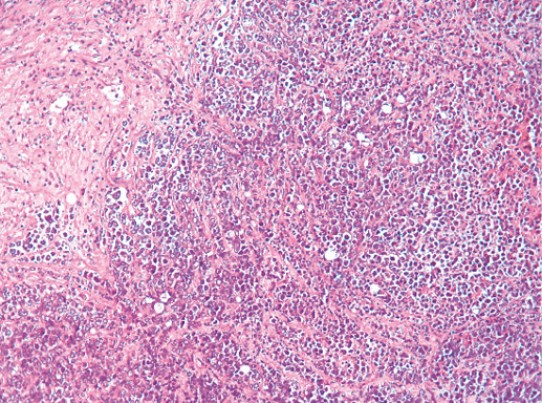
Изучение ранних стадий развития рака выявило потерю гетерозиготности 16q-региона и экспрессию Е-кадгерина в смешанном протоково-дольковом раке и дольковом раке in situ. Это может быть важным для понимания онкогенеза РМЖ и свидетельствует о реальном предшественнике инвазивного рака. Помимо указанных геномных изменений отмечена потеря ряда других, соседних с 16q, локусов.
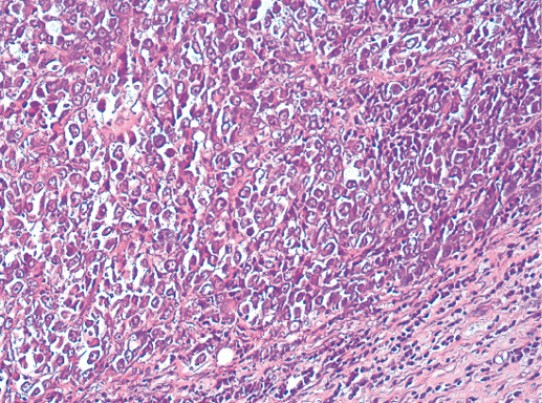
Диагностика фибросаркомы
Лечение фибросаркомы должно проходить под контролем специалиста. Доктор ознакомится с симптоматикой, проведет диагностику. Задача онколога во время беседы с пациентом определить, проявлялась ли подобная симптоматика у родственников. Первый этап осмотра – пальпация, после диагностика переходит на применение инструментов, оборудования, проведение лабораторных анализов.
Среди основных методов диагностики выделяют:
- МРТ. Проводится для определения размеров опухоли, формы, наличия метастазов;
- компьютерная томография, благодаря которой удается определить наличие опухоли в костной ткани;
- биопсия. Взятие ткани для проведения исследования, позволяющего понять строение фибросаркомы;
- иммунотерапия. Проводится для определения наличия антител, из опухоли делается срез.
Пациенту назначается обследование всех органов, для этого используется ультразвуковое исследование. Это дает возможность понять, насколько распространились метастазы.